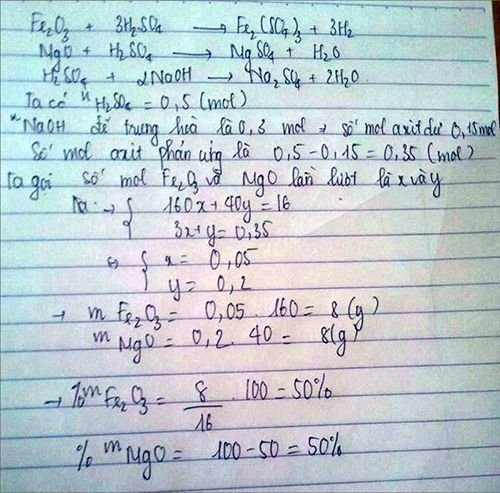Lấy 16g hh MgO và Fe2O3 tan hết trong 0,5 l dd H2SO4 1M sau pu để trung hoà axit còn dư bằng 50g dd NaOH tính % klg mỗi axit trong hh

Những câu hỏi liên quan
Lấy 16g hh MgO và Fe2O3 tan hết trong 0,5 l dd H2SO4 1M sau pu để trung hoà axit còn dư bằng 50g dd NaOH tính % klg mỗi axit trong hh
16g hh gồm MgO và Fe2O3 hòa tan hết trong 0,5l dd axit sunfuric 1M. Sau pư để trung hòa lượng axit còn dư cần 50g dd NaOH 24% Tính % lượng oxit trong hh
LẤY 6 g hh MgO và Fe2O3 tan hết trong 0,5 l dD H2SO4 1M sau phản ứng để trung hòa axít còn dư bằng 50 g dd NAOH 24% tính khối lượng phần trăm mỗi axít trong hh ban đầu
Cho 16 g hỗn hợp MgO , Fe2O3 tan hết trong 0,5 l dd H2SO4 1M .Sau phản ứng trung hòa axit còn dư bằng 50g NaOH 24% .Tính % mỗi axit
\(PTHH:2NaOH+H_2SO_4\rightarrow Na_2SO_4+2H_2O\)
\(n_{NaOH}=\frac{50.24}{100.40}=0,3\left(mol\right)\)
\(PTHH:MgO+H_2SO_4\rightarrow MgSO_4+H_2O\)
\(PTHH:Fe_2O_3+3H_2SO_4\rightarrow Fe_2\left(SO_4\right)_3+3H_2O\)
\(n_{MgO}=x;n_{Fe_2O_3}=y\\ hpt:\left\{{}\begin{matrix}40x+160y=16\\x+3y=0,5.1-\frac{0,3}{2}\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,2\\y=0,05\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{MgO}=\frac{0,2.40}{16}.100\%=50\%\\\%m_{Fe_2O_3}=100-50=50\%\end{matrix}\right.\)
Đúng 0
Bình luận (0)
Xem thêm câu trả lời
16g hỗn hợp gồm Fe2O3 và MgO đc hòa tan hết = 300ml axit HCl. Sau PƯ cần trung hòa lượng axit dư = 50g dd Ca(OH)2 14,8% sau đó đem đun cạn dd nhận đc 46,35g muối khan. Tính % klg mỗi oxit trong hỗn hợp và nồng độ mol của axit HCl
Fe2O3 + 6HCl \(\rightarrow\)2FeCl3 + 3H2O (1)
MgO + 2HCl \(\rightarrow\)MgCl2 + H2O (2)
Ca(OH)2 + 2HCl \(\rightarrow\)CaCl2 + 2H2O (3)
nCa(OH)2=\(\dfrac{50.14,8\%}{74}=0,1\left(mol\right)\)
Theo PTHH 3 ta có:
nCa(OH)2=nCaCl2=0,1(mol)
2nCa(OH)2=nHCl=0,2(mol)
mCaCl2=111.0,1=11,1(g)
mmuối của Mg,Fe=46,35-11,1=35,25(g)
Đặt nFe2O3=a
nMgO=b
Ta có:
\(\left\{{}\begin{matrix}160a+40b=16\\325a+95b=35,25\end{matrix}\right.\)
=>a=0,05;b=0,2
mFe2O3=160.0,05=8(g)
%mFe2O3=\(\dfrac{8}{16}.100\%=50\%\)
%mMgO=100-50=50%
Từ 1 ta có:
6nFe2O3=nHCl(1)=0,3(mol)
2nMgO=nHCl=0,2(mol)
=>\(\sum\)nHCl=0,3+0,2+0,2=0,7(mol)
CM dd HCl=\(\dfrac{0,7}{0,3}=\dfrac{7}{3}M\)
Đúng 1
Bình luận (3)
1. Hh gồm ZnO,MgOnặng 0.3g tan hết trong 17ml dd HCl 1M. Để trung hòa axit dư cần dùng 8 ml dd NaOH 05M. Tính % kl mỗi oxit2. 1 hh gồm Al, CuO cho vào dd Hcl dư thu được 3.72l khí. Mặt khác nếu cho hh trên vào dd NaOH 1M vừa đủ thấy thoát ra V khí H2 và thể tích dd NaOH cần dùng là 500ml. Tìm V3. Cho hoàn toàn 10 gam hh gồm Al, Al2O3 , Cu vào dd HCl dư thu được 3.36 lít khí, nhận dd A rắn B. Đốt A trong không khí đc 2.75 gam rắn Ca/ Tính klg mỗi chất trong hhb/ Nếu cho hh trên vào dd NaOH vừa đủ...
Đọc tiếp
1. Hh gồm ZnO,MgOnặng 0.3g tan hết trong 17ml dd HCl 1M. Để trung hòa axit dư cần dùng 8 ml dd NaOH 05M. Tính % kl mỗi oxit
2. 1 hh gồm Al, CuO cho vào dd Hcl dư thu được 3.72l khí. Mặt khác nếu cho hh trên vào dd NaOH 1M vừa đủ thấy thoát ra V khí H2 và thể tích dd NaOH cần dùng là 500ml. Tìm V
3. Cho hoàn toàn 10 gam hh gồm Al, Al2O3 , Cu vào dd HCl dư thu được 3.36 lít khí, nhận dd A rắn B. Đốt A trong không khí đc 2.75 gam rắn C
a/ Tính klg mỗi chất trong hh
b/ Nếu cho hh trên vào dd NaOH vừa đủ. Tính Vdd NaOH đã dùng
Giai3 hệ phương trình nha mấy bạn! Thanks nhìu!
hòa tan hoàn m g hh fe2o3 và feo bằng 300ml đ chứa đồng thời hcl 1m và h2so4 0,5m đc đ x để trung hòa lg axit dư trong x cần 100 ml dd naoh 1mcòn nếu cho x td vs baoh 2 dư thì 55,45g kt tính m
cho 16g hh fe3o4 hòa tan hết bằng 300 ml dd hcl . sau pứ trung hòa lượng axit dư thì cần dùng 50g ca(oh)2 14,8% , dd thu đc sau pứu cùng chứa 46, 35g muối , tính % khối lượng các oxit trong hh ban đầu , tính Cm dd hcl ban đầu
Cho 16g hỗn hợp gồm Fe2O3 và MgO được hòa tan hết bằng 300ml đ HCl. Sau pứ cần dung hòa axit còn dư bằng 50g dd Ca(OH)2 nồng độ 14,8%, sau đó đem cô cạn dd được 46,35g muối khan.
a, Tính % khối lượng mỗi oxit trong hh ban đầu
b, Tính nồng độ mol/l của dd HCl
a) MgO + 2HCl → MgCl2 + H2O (1)
Fe2O3 + 6HCl → 2FeCl3 + 3H2O (2)
\(n_{Ca\left(OH\right)_2}=\frac{14,8\%.50}{40+17.2}=0,1\left(mol\right)\)
2HCldư + Ca(OH)2 → CaCl2 + 2H2O
0,2 0,1 0,1
\(m_{CaCl_2}=0,1.\left(40+35,5.2\right)=11,1\left(g\right)\)
⇒\(m_{FeCl_3}\) \(_{và}\) \(_{MgCl_2}\) = \(46,35-11,1=35,25\left(g\right)\)
gọi x, y lần lượt là số mol của Fe2O3 và MgO
theo pthh (1) và (2) thì
\(n_{MgCl_2}=n_{MgO}=y\)
\(n_{FeCl_3}=2n_{Fe_2O_3}=2x\)
ta có phương trình \(\left\{{}\begin{matrix}160x+40y=16\\325x+95y=35,25\end{matrix}\right.\)
⇒ x = 0,05; y = 0,2
⇒ \(\%m_{Fe_2O_3}=\frac{0,05.160}{16}.100=50\%\)
⇒ \(\%m_{MgO}=50\%\)
b) nHCl = 6x + 2y + 0,2 = 0,9 (mol)
⇒ C%HCl = \(\frac{0,9}{0,3}=3\left(M\right)\)
Đúng 0
Bình luận (0)
\(n_{Fe_2O_3}=x;n_{MgO}=y\\ PTHH:Fe_2O_3+6HCl\rightarrow2FeCl_3+3H_2\\ PTHH:MgO+2HCl\rightarrow MgCl_2+H_2O\\PTHH:2HCl+Ca\left(OH\right)_2\rightarrow CaCl_2+2H_2O\\ \)
\(n_{Ca\left(OH\right)_2}=\frac{50.14,8}{100.74}=0,1\left(mol\right)\\ \rightarrow n_{HCl.du}=0,1.2=0,2\left(mol\right)\\ \rightarrow m_{CaCl_2}=0,1.111=11,1\left(g\right)\\ \rightarrow325x+95y+11,1=46,35\\ \Leftrightarrow325x+95y=46,35-11,1=35,25\)
\(hpt:\left\{{}\begin{matrix}160x+40y=16\\325x+95y=35,25\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,05\\y=0,2\end{matrix}\right.\)
\(\left\{{}\begin{matrix}\%m_{Fe_2O_3}=\frac{160.0,05}{16}.100\%=50\%\\\%m_{MgO}=100-50=50\%\\\sum n_{HCl}=6x+2y+0,2=0,9\left(mol\right)\rightarrow C_M=\frac{0,9}{0,3}=3\left(M\right)\end{matrix}\right.\)
Đúng 0
Bình luận (0)
Tham khảo!
Câu hỏi của Phạm Hải - Hóa học lớp 9 | Học trực tuyến
Câu hỏi của Lê Anh Ngọc - Hóa học lớp 8 | Học trực tuyến
Good luck!
Đúng 0
Bình luận (0)
Xem thêm câu trả lời